深度解码“9号文”:创新药定价机制重塑背后的投资范式转移
2024年4月15日,国办发布《关于健全药品价格形成机制的若干意见》,这份被业界称为“9号文”的纲领性文件,首次在国家层面明确提出“创新药首发自主定价”。文件发布当日,创新药板块多股涨停,百济神州、荣昌生物等龙头企业涨幅居前。市场为之振奋,但冷静分析后我发现:这是一次结构性分化的起点,而非行业整体性利好。
定价权放开:表象与实质的剥离
初看“9号文”,最直观的感受是药企获得了更大的定价自主权。但仔细研读文件全文后,我意识到这层“利好”背后隐藏着严苛的准入门槛。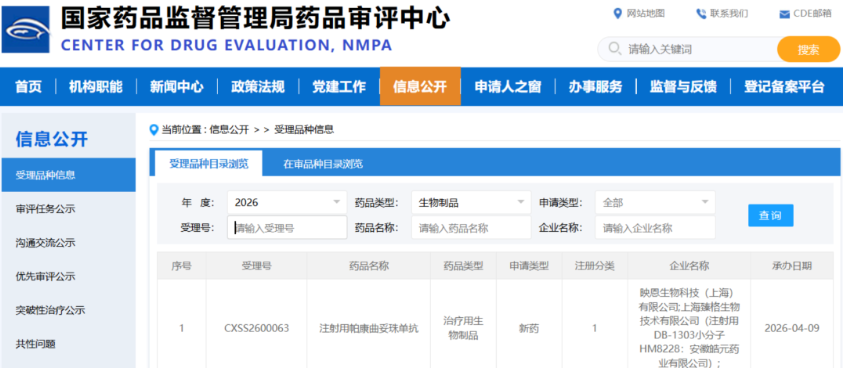
文件明确将新上市药品划分为三个层级:高水平创新药、改良新药、通用名药(即仿制药),并对其实施差异化定价策略。对创新程度高、临床价值大的高水平创新药,政策支持其在上市初期制定与高投入、高风险相符的价格,并在一定时期内保持价格相对稳定。而改良新药和其他仿制药,则被引导制定与患者获益或参照同类药品合理定价。
这意味着,所谓的“自主定价权”并非无限制的自由定价,而是需要药企“自证价值”——综合临床价值、市场供求、竞争格局、社会承受能力等因素,接受社会监督和同行评议。
动态定价机制:价值验证的长期命题
更重要的是,“9号文”打破了“一次定价、终身锁定”的传统模式,建立了动态价格调整机制。
一方面,药企需根据真实世界研究结果和临床使用实效,在首发价格基础上适当调整价格水平。另一方面,医保支付标准将对药品价格形成引导作用,独家药品需通过谈判形成与药品临床价值相匹配的支付标准。此外,文件还提出建立药品医保价值评估制度,支持根据真实世界研究动态调整价格。
简言之,首发高定价只是起点,能否持续获得支付认可,关键在于能否持续提供“临床价值”。
投资范式转移:从β到α的跨越
基于上述分析,我总结出三条核心筛选标准,用于捕捉真正具备定价优势的高价值标的:
第一,平台型创新龙头。这类企业不止于单一爆款,而是建立了可重复、平台化的研发体系。百济神州是典型案例:其BTK抑制剂泽布替尼通过全球“头对头”优效试验改写治疗指南,成为“十亿美元分子”;PD-1替雷利珠单抗凭借Fc段改造的差异化设计获中美欧多国批准。公司已实现全年盈利,验证了其平台化研发体系的可持续性。
第二,全球BD背书的潜力公司。巨额对外授权交易是国际药企对其创新能力的最强背书。2025年,科伦博泰生物与默沙东达成3次合作,涉及9款ADC药物,总交易金额超过110亿美元,刷新中国创新药对外授权纪录。默沙东的投入本质是对科伦博泰OptiDC™ADC平台潜在最佳价值的提前定价认可。
第三,临床数据即将兑现的黑马。这类公司拥有全球首创或潜在同类最佳的差异化管线,关键临床数据将在2026年密集读出。映恩生物尚未有产品上市,但其核心产品帕康曲妥珠单抗(DB-1303)已于2026年4月向中国CDE申报上市,用于HER2阳性乳腺癌。这是其首个申报上市的创新药产品,即将开启商业化从0到1的突破。
事件驱动框架:催化剂跟踪方法论
在上述筛选标准基础上,我建立了以“临床数据”为核心的事件驱动跟踪框架。
首先,紧盯顶级学术会议日历。2026年第二、三季度的美国癌症研究协会(AACR)、美国临床肿瘤学会(ASCO)等会议,将是数据读出的重要窗口期。
其次,聚焦核心管线的关键进展。康方生物依沃西在非小细胞肺癌领域与K药的全球头对头研究数据(预计2026Q2读出),以及君实生物全球首创BTLA单抗的III期临床进展,都将是触发价值重估的关键催化剂。
结论与建议
“9号文”的发布,标志着中国创新药行业从“控费压价”进入“价值定价、激励创新”的新阶段。在此背景下,投资者需规避三类企业:产品同质化严重、依赖跟随式研发的标的;缺乏明确临床差异化优势、难以支撑支付谈判的标的;管线热闹但缺乏全球开发和商业化能力的标的。
政策红利只属于那些能通过全球数据验证自身“高临床价值”的标杆企业。投资时需回归创新本质,精选个股阿尔法,而非追逐行业β。